原文轉自奇點網
我從來沒想過,強力致癌基因ALK 還會這樣的形像出現在我的面前。
今天,頂級期刊《細胞》雜誌刊登了澳大利亞科學院Josef M. Penninger團隊,聯合瑞士Nestle健康科學研究所Nele Gheldof和Jorg Hager團隊做出的重要研究成果。
他們發現,ALK 基因中的一個突變,竟然與健康年輕人體型消瘦,怎麼都吃不胖相關。他們隨後在模式動物中做的遺傳學研究發現,下丘腦神經元中表達的ALK ,竟然能通過交感神經調控脂肪的分解。敲除ALK基因之後,即使讓小鼠長期吃高脂飲食,依然長不胖 [1]。
研究人員認為,他們的研究表明,癌基因ALK 還是個“瘦身基因”。

▲ 論文首頁截圖
如果你留意觀察,在你周圍一定有這樣兩類人:一類無論怎麼少吃多運動都不見瘦;另一類無論怎麼多吃不運動都長不胖。這兩類人互相嫉妒。
Penninger等注意到,目前已經有很多關於肥胖的研究,也發現了很多與肥胖有關的基因位點,不過只有屈指可數的幾個基因被證實是肥胖易感基因;此外鮮有研究探索體型消瘦的遺傳學問題。
Penninger團隊決定走鮮有人走的那條路,去探索下瘦子為什麼總是那麼瘦的問題。說不定能曲線解決胖子們的煩惱。

▲ Josef M. Penninger
Penninger等找到了愛沙尼亞生物庫(EGCUT),從中提取了兩類年齡在20到44歲之間的人的數據:一類是瘦子,他們是BMI持續在處於最低的6%,且沒有進行性脂肪營養不良和神經性厭食症等疾病的人,經過年齡和性別的調整,這部分人的BMI通常在18以下;第二類是對照組,BMI在30-50百分位數之間。
最終,瘦子有881人,僅佔整個數據庫的1.9%左右,這說明這類人真是不多。對照組有3173人。

▲ 研究方式
隨後研究人員就基於上面的數據,開展GWAS研究。通過一番比對分析,最終找到了5個與體型消瘦有關的變異位點。有兩個位於基因之間( ICE1和MED10 , FOS和TMED10之間),兩個位於基因裡面( DEPTOR和ALK ),另外一個在一個未定性的長非編碼RNA裡面。
無論是誰,看到上面的五個基因位點都會大吃一驚。因為大名鼎鼎的癌基因ALK 竟然赫然在列。
顯然, ALK的出現,也吸引了Penninger團隊的注意。他們迅速分析了ALK這種變異在其他人群中的情況。結果發現除了非洲血統的人群比較少見之外,歐洲、亞洲和美洲人群中都算比較常見。
考慮到之前關於ALK的研究主要涉及到癌症,科學家對ALK是否存在其他生理功能幾乎一無所知,Penninger團隊察覺,他們的這個發現,或許能讓我們對ALK有全新的認知。

▲ 五個突變
為了心裡能有個底,Penninger團隊首先基於RNAi技術,在能快速生長和繁殖的果蠅中迅速做了個驗證實驗。沉默果蠅的ALK基因之後,果蠅的甘油三酯水平顯著降低,代謝調節也出現異常。
隨後,研究人員又在這個數據庫,以及其他的數據庫中做了深入的關聯分析,發現上面挖到的5個基因位點裡面,只有兩個與代謝性狀相關。讓研究人員感到興奮的是,ALK 的變異位點,居然與BMI、血漿甘油三酯水平、血漿低密度脂蛋白膽固醇水平、葡萄糖平衡、血漿脂蛋白水平和糖化血紅蛋白等多個代謝性狀密切相關。
如此看來, ALK 這個基因真的有可能與長不胖有關係。小鼠實驗可以安排上了。
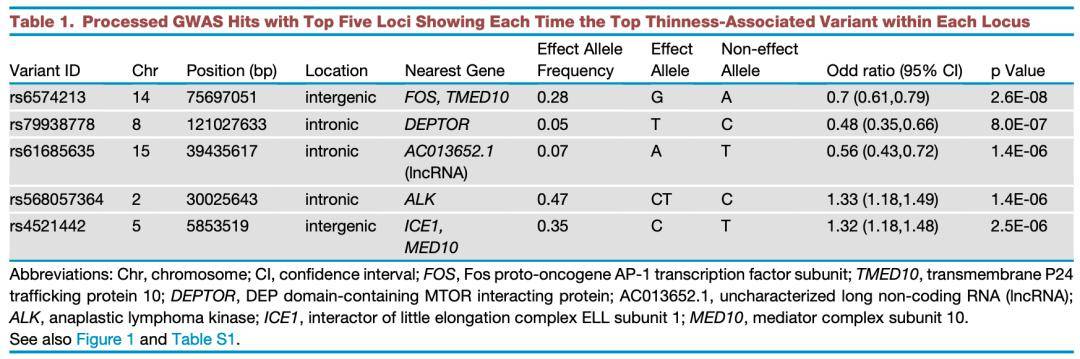
▲ 快看看你的ALK有沒有這樣的突變
我這裡簡單介紹一下ALK ,熟悉的朋友可以跳過不看。
ALK 的中文名叫間變性淋巴瘤激酶,它最早是因為和其他的基因發生重排出現過度激活,導致腫瘤的發生才被科學家揪出來的。
目前科學家已經在包括神經母細胞瘤和非小細胞肺癌在內的多種腫瘤,發現了20多種ALK重排和突變[2]。ALK重排目前是治療癌症的一個重要靶點,相關藥物已經投入臨床使用。
由於ALK主要在大腦中表達,因此它也被認為在神經系統的發育和功能中發揮很重要的作用。但遺憾的是,ALK基因被敲除的小鼠,除了出現了微妙的行為變化之外,其他各方面似乎都沒有觀察到顯著的變化。
只有一個研究記錄到ALK 缺陷型小鼠體重似乎出現下降[4],但是做這個研究的科學家沒有太關注這個現象。這也就給Penninger團隊留下了一個深入研究ALK 生物學功能的機會。

▲ 該圖片由Deedee86在Pixabay上發布
於是Penninger和他的同事們構建了ALK 基因缺陷型模式小鼠。他們發現這種缺陷型小鼠,在各方面與野生型小鼠相比,確實沒有顯著的差異。各方面都正常,說明敲除ALK 基因對小鼠的生理和生命活動沒有影響,或者影響甚微。
不過,用正常飲食餵養一段時間之後,ALK基因缺失小鼠更瘦,脂聯素(脂肪細胞分泌的一種胰島素增敏激素)水平增加,血糖平衡也有所改善;不過小鼠的食物攝入量和活動量與野生小鼠相比沒什麼顯著差異。
為了檢驗ALK 基因缺失小鼠是不是怎麼都吃不胖,Penninger團隊給這些小鼠餵了16週的高脂食物,讓它們吃進去的熱量超標。
讓研究人員感到興奮的是,敲除ALK基因有很強的抗肥胖作用。ALK基因正常的小鼠像吹了氣一樣,而沒了ALK基因的小鼠,身材保持的非常好。
研究人員還注意到,即使是小鼠只出現一個ALK 等位基因缺失,仍有很好的抗肥胖作用。這就意味著這裡面還有個基因劑量效應。不過這種情況下保護作用究竟有多少,研究人員沒有給出具體數據。

▲ 高脂飲食的不同效果
MRI分析顯示,與正常小鼠相比,ALK基因缺失的小鼠瘦肉質量正常,只是脂肪大量減少了,而且脂肪細胞也比較小。不過缺失小鼠和正常小鼠食物的攝入量沒有差異,腸道對營養的吸收也沒有差異。
為了解開ALK缺失小鼠抗肥胖的原因,Penninger和他的同事分析了小鼠的能量支出(EE)狀況。沒了ALK基因之後,小鼠每日能量支出顯著升高。
原來吃進去的都產熱了~

▲ 能量支出比較
ALK 又是如何調節機體產熱的呢?
在本研究中,Penninger團隊發現, ALK 主要在小腦,特別是下丘腦中樞神經中表達,其他與代謝有關的組織器官幾乎檢測不到ALK 的表達。這也與之前的研究類似。
深入的研究發現,消除下丘腦神經元產生的ALK ,會促進交感神經產生更多的去甲腎上腺素(NE)。研究人員也在身體偏瘦的人群中[5]發現去甲腎上腺素水平升高的現象。
而去甲腎上腺素的功能早就有相關的研究,它一方面可以誘導脂肪組織中的脂肪分解 [6],另一方面還可以促進脂肪組織褐變 [7],變成燃脂的棕色脂肪。Penninger和他的同事在本研究中也證實了這兩點。
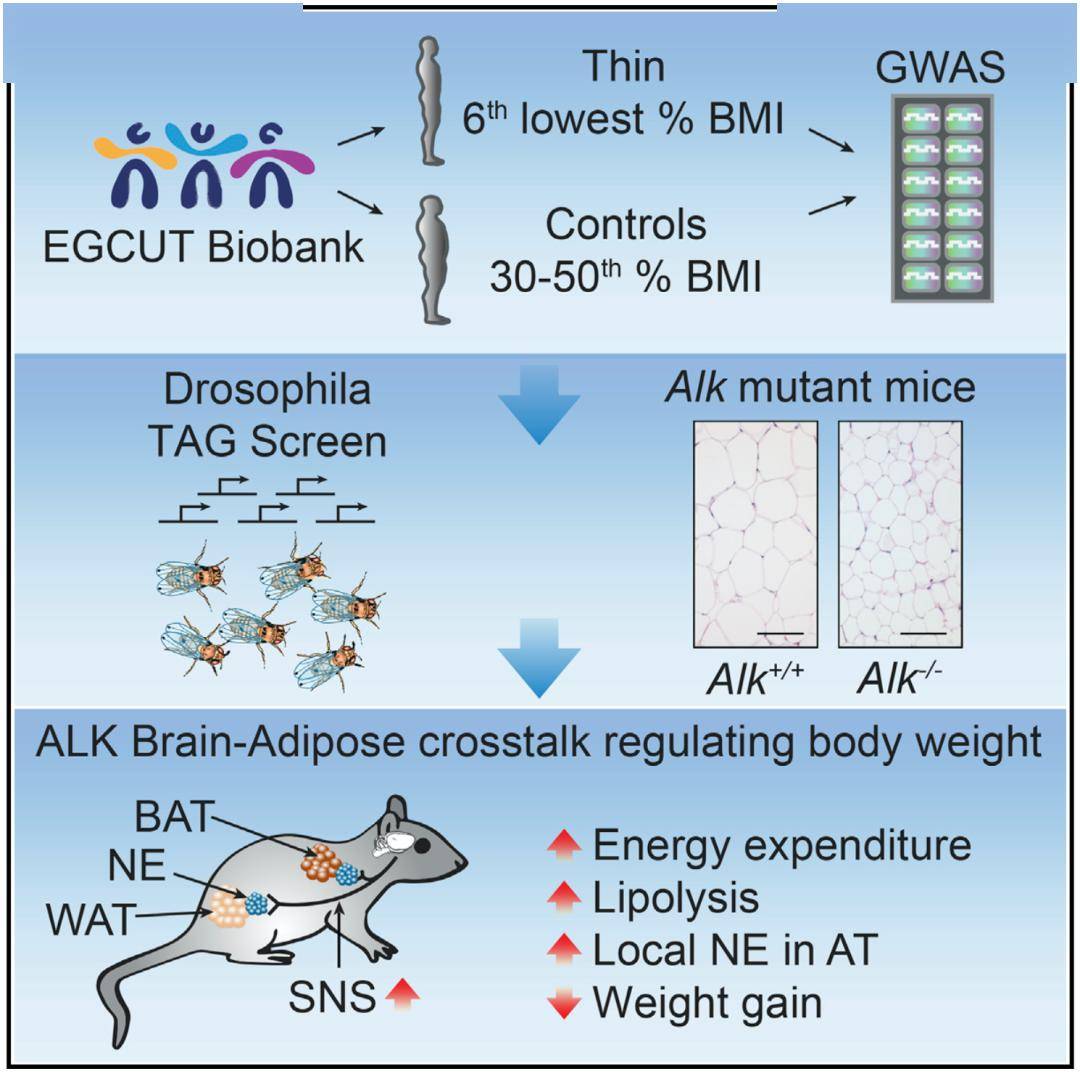
▲ 研究過程匯總一覽
最後來總結一下,這個研究從多個角度證明了ALK 是個瘦身基因, ALK 的失活突變會讓哺乳動物對肥胖產生抵抗力。這主要是通過作用於交感神經,促進脂肪的消耗實現的。
由於目前靶向ALK的抑製劑已經用於治療癌症,Penninger表示,他們將來會研究這些藥物是否有減肥效果 [8]。
儘管如此,奇點糕還是強烈不推薦大家去嘗試。這畢竟是個基礎研究,離臨床應用還有很大的距離。退一萬步說, ALK抑製劑可是抗癌藥呢~
不過,如果大家已經做過基因檢測的話,不妨去看看自己的ALK 有沒有攜帶這個突變,或者其他的失活突變。
編輯神叨叨
[1].https://www.cell.com/cell/fulltext/S0092-8674(20)30497-9
[2].Della Corte CM, Viscardi G, Di Liello R, et al. Role and targeting of anaplastic lymphoma kinase in cancer[J]. Molecular cancer, 2018, 17(1): 30.
[3].Vernersson E, Khoo NKS, Henriksson ML, et al. Characterization of the expression of the ALK receptor tyrosine kinase in mice[J]. Gene Expression Patterns, 2006, 6(5): 448-461.
[4].Bilsland JG, Wheeldon A, Mead A, et al. Behavioral and neurochemical alterations in mice deficient in anaplastic lymphoma kinase suggest therapeutic potential for psychiatric indications[J]. Neuropsychopharmacology, 2008, 33(3): 685-700.
[5].Ling Y, Carayol J, Galusca B, et al. Persistent low body weight in humans is associated with higher mitochondrial activity in white adipose tissue[J]. The American journal of clinical nutrition, 2019, 110(3): 605-616.
[6].Bartness TJ, Liu Y, Shrestha YB, et al. Neural innervation of white adipose tissue and the control of lipolysis[J]. Frontiers in neuroendocrinology, 2014, 35(4): 473-493.
[7].Harms M, Seale P. Brown and beige fat: development, function and therapeutic potential[J]. Nature medicine, 2013, 19(10): 1252.
[8].https://www.genomeweb.com/microarrays-multiplexing/alk-gene-linked-natural-thinness-genetic-functional-studies#.XseIvBMzbOQ




