[vc_row][vc_column][vc_column_text]
近日,《英國血液病雜誌》(British Journal of Haematology)在線發表了一篇題為“SARS-COVID-2病毒引起霍奇金淋巴瘤緩解”的一個病例。
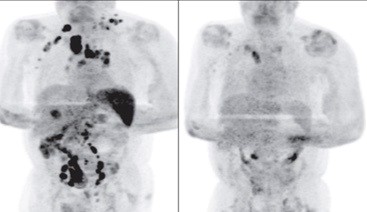
61歲,男性,因進行性淋巴結腫大和體重減輕轉到血液科。因繼發於IgA腎病的終末期腎衰竭而接受血液透析。腎移植失敗後,他已經停止免疫抑制治療3年了。鎖骨上淋巴結穿刺活檢顯示為EB病毒陽性的經典霍奇金淋巴瘤[EB病毒聚合酶鏈反應(PCR) 4800 copies/ml;log10 3·68]。FDG-PET/CT 評估患者屬於IIIs期(左圖)。
左圖:剛確診晚期霍奇金淋巴瘤時的PET/CT成像,右圖:4個月後復查的PET/CT成像,腫瘤幾乎完全消失
這例患者的病史比較複雜,原本患有嚴重的腎病,因IgA腎病繼發性終末期腎衰竭一直在做血液透析。患者接受過腎移植,但是遭遇了失敗。
自腎移植失敗,該患者停止免疫抑制治療約有三年時間。之後,因出現淋巴結腫大和體重減輕等症狀入院治療,患者被確診為EB病毒(Epstein-Barr virus, EBV)為陽性的晚期霍奇金淋巴瘤。
在檢測出患有淋巴瘤後,該患者因呼吸困難再次入院,並被確診患有新冠。到此,男子的身上出現了三種疾病:末期腎衰竭,晚期癌變的霍奇金淋巴瘤,以及新冠肺炎。這任何一種疾病放在一位61歲老人的身上都是十分凶險的,不難想像他那時所承受的煎熬和病痛。
住院11天后,男子的症狀有所緩解,決定回家休養。或許在他看來,放棄治療未嘗不可。事實也是如此,男子在回到家後再也沒有接受過任何皮質類固醇和免疫化療。
4個月後,該患者回醫院複查淋巴瘤,PET-CT顯示他體內的腫瘤絕大多數都消失了,而且相關的腫瘤標記物也下降了90%以上。
發生在男子身上的狀況讓研究人員感到不可思議。目前,研究人員推測認為,有可能是新冠病毒觸發了人體抗腫瘤的免疫反應,類似於溶瘤病毒治療癌症。這一案例也提示了新冠病毒未來將有可能在經過改造後,成為一種新型的“溶瘤病毒療法”。
說得直接一點,新冠感染激活了抗腫瘤的免疫反應,在殺滅病毒的同時,也殺死了癌細胞。
歷史上也出現過其它類似的病例。如,2012年Clinical Lymphoma, Myeloma & Leukemia發表的一篇文章曾提過一位上頜竇瀰漫性大B細胞淋巴瘤患者在並發肺炎和艱難梭菌性結腸炎之後,腫瘤同樣逐漸消退的情況。當時的研究者猜測,抗腫瘤免疫反應可能是導致腫瘤自發緩解的潛在原因。
儘管目前尚不清楚病毒導致淋巴瘤患者腫瘤消退的具體機制,但是這些報告有助於未來研究人員挖掘出更有效的癌症免疫療法。
不過,研究人員還是補充指出,這並不代表新冠病毒可以治療癌症,畢竟這樣的案例十分少見。
但是這裡要強調的是,癌症患者可千萬不要故意感染新冠病毒。
全球已經有很多癌症患者感染新冠病毒,但這是目前報導的第一例腫瘤消失,獲益是極個例。感染新冠會給癌症患者帶來更大的身體負擔,也會帶來危及生命的風險。
溶瘤病毒被定義為基因工程或天然存在的病毒,其可以選擇性地進行病毒複製並殺死腫瘤細胞而不傷害健康組織。
溶瘤病毒主要通過選擇性腫瘤細胞殺傷和抗腫瘤免疫的雙重殺瘤機制來實現治療功效。其中,腫瘤選擇性由幾個因素驅動:
①溶瘤病毒通過病毒特異性受體介導的機制進入細胞。通常,在腫瘤細胞上高度表達特定的病毒進入受體。另外,還有通過重新靶向溶瘤病毒以通過腫瘤特異性受體進入細胞來改善腫瘤選擇性的努力。
②與正常靜止細胞相比,腫瘤細胞具有高代謝和復制活性,快速細胞分裂增加了病毒複製。此外,腫瘤驅動突變特異性地增加了腫瘤細胞中病毒複製的選擇性。
③許多腫瘤細胞具有抗病毒I型乾擾素信號傳導的缺陷,因此支持選擇性病毒複製。
最後,腫瘤微環境中病毒複製會促使先天免疫和適應性免疫激活。這種激活限制了病毒在正常細胞中的傳播;重要的是,病毒的存在以及細胞裂解、腫瘤抗原的釋放和危險相關的分子模式,可以克服腫瘤微環境中的免疫抑制並促進抗腫瘤免疫。
溶瘤病毒療法所使用的病毒類型主要有皰疹病毒(HSV)、腺病毒(Ad)、麻疹病毒(MeV)、牛痘病毒(VV)、呼腸弧病毒、細小病毒(PV)、逆轉錄病毒等。根據病毒的遺傳物質不同,又可以分為DNA病毒和RNA病毒兩種類型。目前研究最多的是皰疹病毒、牛痘病毒、腺病毒。
➤皰疹病毒(Herpesvirus, HSV)是一種有包膜的、嗜神經性的雙鏈DNA病毒。其基因組較為龐大,適合進行較大的基因片段插入;同時其複制能力較強更好的殺傷腫瘤細胞;易於設計,可以共表達非病毒基因來增強治療效果;具有不會引發炎症和免疫反應等優勢。
➤牛痘病毒(Vaccinia virus, VV)是一種雙鏈DNA病毒,具有長約190kbp的基因組,是一個很大的DNA病毒。牛痘病毒和其它病毒不同的是,牛痘病毒有兩種形態,無包膜的IMV和有包膜的EEV。
優點:複製速度很快;基因組不整合到宿主細胞染色體中,不會引起插入致突變性;基因組很大,可以插入大段的外源基因(表達治療劑)。
➤腺病毒(Adenovirus, Ad)一種無包膜的雙鏈DNA病毒。由腺病毒改造而成的各類溶瘤腺病毒,被稱為條件複製型/複製選擇性腺病毒具備許多優勢,包括:感染細胞範圍廣泛,幾乎能感染所有類型的細胞;基因組不整合到宿主細胞染色體中,不會引起插入致突變性;病毒滴度高,容易於製備和純化等。
但腺病毒作為溶瘤病毒也存在一些缺點,包括:自身免疫原性強,易引起機體對腺病毒本身的免疫排斥;另外有研究表明,腺病毒靜脈注射容易在肝臟富集,引起毒副作用等。
目前,嚴格來說上市的溶瘤病毒產品只有2015年FDA批准的Amgen(安進)公司的T-vec(Imlygic,I型單純皰疹病毒),用於黑色素瘤患者的局部治療。大量的溶瘤病毒的研發處於臨床試驗階段,其中大部分處於早期臨床階段。
不過,近些年來,溶瘤病毒的開發展現出強大的潛力,也是癌症治療非常熱門的方向。我國也湧現了一大批優秀的企業,包括亦諾微、天士力創世傑、濱會生物、中生復諾健、威溶特、養生堂、錘特生物等。
另外,科學家們也在不斷探索新的毒株用於溶瘤病毒療法的開發。
➤ 牛病毒性腹瀉病毒(Bovine pestivirus, BVDV)
2020年7月,《血液與腫瘤學雜誌》上發表了一項研究,意大利的研究人員首次研究了牛病毒性腹瀉病毒(BVDV)作為溶瘤病毒療法用於多發性骨髓瘤(MM)。研究發現,BVDV結合CD46受體,具有顯著的抗MM活性。
BVDV是牛血清攜帶的最常見的外源病毒之一,是一種牛病原體,曾經有報導發現該病原體出現在人用生物製品的牛源原料中,並且許多國家都存在BVDV的牛群感染與流行。但研究發現,BVDV並不會導致人類產生疾病,因而該病毒被考慮用作治療人類疾病的非人類病原體病毒,即溶瘤病毒。
在2020年11月開展的第35屆腫瘤免疫治療學會年會(SITC 2020)上,OncoMyx公開了其根據兔子體內的一種兔痘病毒——粘液瘤病毒,開發的溶瘤病毒療法的積極的臨床前研究數據。
數據表明,通過瘤內註射或靜脈給藥後,該藥物顯著減緩了多種類型的腫瘤生長,並且,與PD-(L)1抑製劑聯合使用時,縮小腫瘤和延長動物壽命的療效更好。
粘液瘤病毒是痘病毒(poxvirus) 家族的一員,且被分類為兔痘病毒屬leporipoxvirus),是一種遺傳物質為雙股螺旋DNA的大型病毒。粘液瘤病毒與其它溶瘤病毒一樣,能夠直接感染腫瘤細胞使其死亡,同時釋放腫瘤抗原,誘導機體對腫瘤細胞進行免疫應答。
其實早在19世紀中葉,就有腫瘤消退與自然病毒感染同時發生的病例,其中最常見的病例是免疫功能顯著抑制相關的血液惡性腫瘤患者。但這些自然病毒所帶來的緩解是短暫的,通常只持續一兩個月。
▲ 4項具有歷史意義的臨床試驗(圖片來源:Molecular Therapy)
這一百多年來,科學家們一直在尋找病毒作為癌症的治療方法,20世紀50年代和60年代掀起了該領域的熱潮。雖然20世紀70年代和80年代較為低迷,但過去的二十年又是一個複興,並最終迎來了溶瘤病毒的首次上市批准。儘管有幾款上市的溶瘤藥物由於療效不佳,沒有得到廣泛的應用,但是對溶瘤病毒的產業還是起到了重要的推動作用。
溶瘤病毒治療並不是一個新發現,但隨著科學研究的進步,科學家們不斷克服了該領域的重重挑戰。根據目前的發展趨勢,溶瘤病毒終將會是癌症治療的下一個重大突破。
https://onlinelibrary.wiley.com/doi/full/10.1111/bjh.17116
https://pubmed.ncbi.nlm.nih.gov/23025990
[/vc_column_text][/vc_column][/vc_row]